Mit der Schere gegen das HI-Virus

Ein Raunen ging durch die Forschergemeinde, als der Dresdner Molekularbiologe Frank Buchholz und der Hamburger Virologe Prof. Dr. Joachim Hauber im Februar 2016 mit ihrem Projekt an die Öffentlichkeit gingen. Mit dem umprogrammierten Enzym mit dem Namen Rekombinase Brec1 könne das HI-Virus aus dem Erbgut entfernt werden. AIDS könnte damit zum ersten Mal wirklich heilbar werden. TOP Gesundheitsforum sprach mit Frank Buchholz über die Chancen der Genom-Chirurgie, die Wirkungsweise des Enzyms und den Fahrplan bis zur Anwendung beim Menschen.
Inwiefern ist die Entwicklung der Genom-Chirurgie eine Voraussetzung für Ihr Projekt?
Frank Buchholz: Da das Erbgut entschlüsselt wurde, kennen wir auch die Erbinformationen. Dadurch können wir bei genetisch bedingten Erkrankungen immer häufiger erkennen, wo die Fehler genau liegen. Die noch junge Genom-Chirurgie tritt nun an, diese Fehler zu reparieren. Das ist natürlich momentan in aller Munde, da es in der Medizin schon einer Revolution gleichkommt und natürlich auch weitreichende gesellschaftspolitische Folgen hat.
Worin besteht nun genau Ihre Arbeit in diesem Zusammenhang?
In gewisser Weise entwickeln wir Methoden und Werkzeuge, mit denen die Genom-Chirurgie arbeiten kann. Dazu gehört auch das Enzym namens Rekombinase Brec1, das DNA an bestimmten Stellen bindet, dort zerschneiden kann und die freien Enden dann aber auch wieder zusammenklebt. Die Analogie von Schere und Kleber ist hier durchaus zulässig. Vereinfacht kann man wirklich sagen, dass wir etwas Schlechtes herausschneiden wollen. Und dieses Enzym versuchen wir nun schon einige Jahre zu entwickeln und zu verbessern.
Warum funktioniert diese Technik gerade bei der Bekämpfung des HI-Virus so gut?
Prinzipiell sind diese Technologien auch auf andere genetische Erkrankungen anwendbar. Wir haben uns dann aber aus verschiedenen Gründen initial für das Hi-Virus entschieden. Das Tückische an dem Virus ist, dass es seine eigenen Erbinformationen in das Erbgut des Trägers einschleust. Dadurch bekommt man den Erreger nicht wieder los, weil er praktisch Teil der jeweiligen Zelle wird und diese gewissermaßen umprogrammiert. Alle der teils sehr guten Medikamente, die es heute gibt, können nur den Befall mit neuen Viren verhindern, aber keine Heilung des sogenannten Provirus herbeiführen. Unsere Überlegung war nun, dass wir das gezüchtete Enzym so programmieren, dass es genau die Sequenzen des Virus im menschlichen Genom findet. Gelingt es, dass die Zelle von den Erbinformationen des Provirus befreit wird, kann man tatsächlich von Heilung sprechen.
Wie bekommt der Patient die Enzyme?
Es ist natürlich keine Standard-Therapie. Man muss zunächst das Blut mit den befallenen Zellen vom Patienten isolieren. Mit einer sogenannten Genfähre wird die Rekombinase dann eingebracht, bevor der Patient seine eigenen Zellen wieder zurückbekommt.
Wie sind Sie auf den Gedanken gekommen, dass sich gerade die Rekombinasen für die Therapie eignen?
Ich habe schon länger an den Rekombinasen geforscht, die ganz natürlich in der Natur vorkommen. Nur erkennen diese ursprünglichen Versionen natürlich keine HIV-Sequenzen. Wir sagten voraus, dass eine umprogrammierte Rekombinase die HIV-Sequenzen erkennen würde.
Wie funktioniert diese Umprogrammierung?
Dafür nutzen wir die sogenannte molekulare Evolution. Im Prinzip ist das eigentlich nichts anderes als eine Züchtung. So wie Tiere mit bestimmten Eigenschaften gezüchtet werden, machen wir das auf molekularer Ebene. Dabei wird die Sequenz des Enzyms immer wieder leicht verändert, durch Mutation und Selektion. Dann suchen wir die besten Rekombinasen heraus und kreuzen diese. So adaptieren wir das Enzym in Richtung der Sequenz, die es schließlich erkennen soll. Und das funktioniert erstaunlich gut.
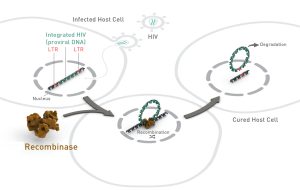
Die infizierte Zelle wird mit dem Enzym Rekombinase vom HI-Virus befreit und geheilt. / Foto: Medizinische Fakultät Carl Gustav Carus, TU Dresden
Können Sie mögliche Nebenwirkungen ausschließen?
Mit den wissenschaftlichen Methoden, die uns zur Verfügung stehen, konnten wir keine Nebenwirkungen feststellen. Man konnte ja durchaus befürchten, dass das Enzym auch an anderen Stellen schneidet. Das ist aber scheinbar nicht der Fall. Allerdings muss man sagen, dass man gerade bei neuen Therapien etwaige Nebenwirkungen nicht restlos ausschließen kann. Deshalb gilt es auch für die kommenden klinischen Studien, dass wir mit sehr viel Bedacht vorgehen müssen. Das ist aber immer bei jedem neuen Medikament so.
Wie ist die Zusammenarbeit mit Prof. Dr. Joachim Hauber vom Heinrich-Pette-Institut in Hamburg entstanden?
Wir studieren das Enzym ja schon seit sehr langer Zeit. Nachdem wir uns dazu entschlossen hatten, die Anwendbarkeit beim HI-Virus zu testen, fehlte uns die Expertise in der Virologie. Und Professor Hauber gehört zu den Koryphäen auf diesem Gebiet. In seinem Labor in Hamburg verfügt er über die nötigen Sicherheitsstandards, die die Arbeit mit solch gefährlichen Viren auch erlauben. Ich bin dann einfach an ihn herangetreten und habe ihm unsere Ergebnisse vorgestellt. Davon war er sehr angetan. Seitdem arbeiten unsere Institute eng zusammen. Alle Vorgänge, die mit den tatsächlichen Viren zu tun haben, finden in Hamburg statt, während wir eher die Enyzm-Entwickler sind.
Wie sieht der Fahrplan für die klinischen Studien aus?
Wir sind gerade in der Phase, in der wir versuchen, die Finanzierung für die klinischen Studien sicherzustellen. Geplant sind die Studien in Dresden und Hamburg. Als bisher letzten Schritt haben wir mit dem Paul-Ehrlich-Institut gesprochen, das für die Genehmigung klinischer Studien und schließlich für die Zulassung biomedizinischer Arzneimittel zuständig ist. Dort haben wir ein Protokoll vorgeschlagen, wo-raufhin wir Signale bekamen, dass eine Studie auf Basis der molekularen Schere genehmigungsfähig wäre. Wenn die Genehmigung dann tatsächlich da ist, müssen wir die Patienten und medizinisches Fachpersonal rekrutieren. Dann braucht es aber noch mehrere klinische Studien mit unterschiedlichen Zielstellungen, bis eine endgültige Therapie entwickelt werden kann, die dann breit anwendbar wäre.
Das Gespräch führte Philipp Demankowski.














